savunmahavacılıkteknolojipolitikaanalizmevduatkriptosağlıkkoronavirüsenflasyonemeklilikötvdövizakpchpmhp

savunma
havacılık
teknoloji
politika
analiz
mevduat
kripto
sağlık
koronavirüs
enflasyon
emeklilik
ötv
döviz
akp
chp
mhp
DOLAR
37,9449
EURO
41,0243
ALTIN
3.819,84
BIST
9.659,48
DOLAR
37,9449
EURO
41,0243
ALTIN
3.819,84
BIST
9.659,48
Adana
Adıyaman
Afyon
Ağrı
Aksaray
Amasya
Ankara
Antalya
Ardahan
Artvin
Aydın
Balıkesir
Bartın
Batman
Bayburt
Bilecik
Bingöl
Bitlis
Bolu
Burdur
Bursa
Çanakkale
Çankırı
Çorum
Denizli
Diyarbakır
Düzce
Edirne
Elazığ
Erzincan
Erzurum
Eskişehir
Gaziantep
Giresun
Gümüşhane
Hakkari
Hatay
Iğdır
Isparta
İstanbul
İzmir
K.Maraş
Karabük
Karaman
Kars
Kastamonu
Kayseri
Kırıkkale
Kırklareli
Kırşehir
Kilis
Kocaeli
Konya
Kütahya
Malatya
Manisa
Mardin
Mersin
Muğla
Muş
Nevşehir
Niğde
Ordu
Osmaniye
Rize
Sakarya
Samsun
Siirt
Sinop
Sivas
Şanlıurfa
Şırnak
Tekirdağ
Tokat
Trabzon
Tunceli
Uşak
Van
Yalova
Yozgat
Zonguldak
Ankara
Hafif Yağmurlu
15°C
Ankara
15°C
Hafif Yağmurlu
Çarşamba
Yağmurlu
13°C
Perşembe
Yağmurlu
13°C
Cuma
Hafif Yağmurlu
13°C
Cumartesi
Yağmurlu
11°C
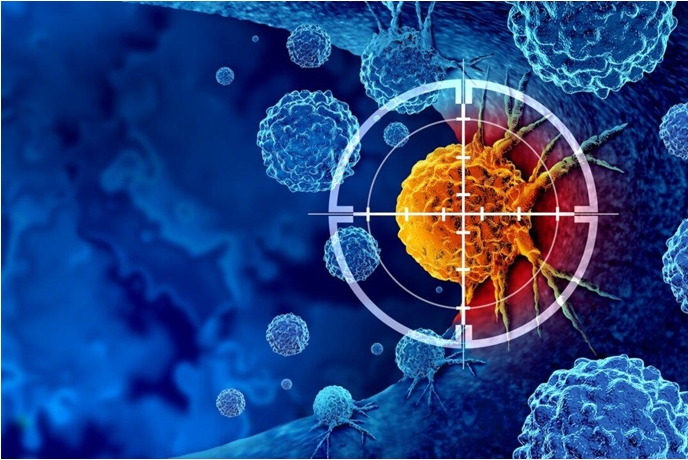
2024 için Altı Yenilikçi Kanser Tedavisi
2024 için Altı Yenilikçi Kanser Tedavisi
Çeviren: Turgay Derya, sunsavunma.net, 1 Ağustos 2024
Araştırmacılar dışkı naklinden darbeli alanlara kadar kanseri temizlemenin yeni yollarını inceliyor.
Ulusal Kanser Enstitüsü’ne göre, Amerika Birleşik Devletleri’nde 17 milyondan fazla insan kanserle yaşıyor ve tedavi maliyetleri 2020’de 200 milyar doları aşıyor. Tıbbi teknolojideki ilerlemeler kanserden ölüm oranlarında düşüşe yol açarken, teşhis edilen vaka sayısı artmaya devam ediyor. Amerikan Kanser Derneği, 2024’ün ABD’de iki milyondan fazla yeni kanser vakasının görüleceği ilk yıl olacağının tahmin edildiğini bildirmektedir.
Yüzyılı aşkın bir süredir, kemoterapi gibi yüksek doz sistemik tedaviler kanser tedavisinin temel taşı olmuştur. Bu ilaçlar bazı hastalar için başarılı olsa da, genellikle bağışıklık sistemini tehlikeye atmakta ve ciddi yan etkilere yol açmaktadır.
Williams Kanser Enstitüsü’nde bütünleştirici bir hekim olan Dr. Nathan Goodyear, sistemik-tümör yaklaşımının nüks ve metastaza katkıda bulunabileceğini açıklıyor. Yenilikçi kanser tedavilerine duyulan ihtiyacın her zamankinden daha kritik olduğunu vurguluyor.
Dr. Goodyear, “Kanser, ya kanser yok olana, ya da birey yok olana kadar sürekli mutasyona uğruyor,” diyerek hastalığın sürekli değişen doğasının altını çiziyor. Kanserle etkin bir şekilde mücadele etmek için yeni ve yenilikçi tedavilerin benimsenmesinin öneminin altını çiziyor.
Dr. Goodyear, “Hasta savunucuları olarak hizmet vermeye devam ettiğimiz sürece, sadece kanserin değişkenliğine ayak uydurmak için değil, kanseri aşmak için de inovasyonun sınırlarını zorlamalıyız” diyor.
Fekal Transplantasyon
Bir zamanlar geleneksel olmayan bir yöntem olarak görülen dışkı nakli, artık umut verici bir kanser tedavisi olarak ortaya çıkmaktadır. Bilimsel olarak fekal mikrobiyota transplantasyonu (FMT) olarak bilinen bu prosedür, sağlıklı bir donörden alınan dışkı maddesinin hastanın gastrointestinal sistemine nakledilmesini içerir. Amaç, kanser hastalarında genellikle kronik antibiyotik kullanımı veya hastalığın kendisi nedeniyle bozulan dengeli bir bağırsak mikrobiyomunu geri kazandırmaktır.
eClinicalMedicine’de yayınlanan 2023 tarihli bir çalışmada, iki immünoterapi ilacıyla birlikte fekal transplantların kullanılmasının, ilerlemiş kolorektal kanserli hastalarda sağkalımı önemli ölçüde artırdığı bulunmuştur. İmmünoterapi, kanserle savaşmak için vücudun kendi bağışıklık sisteminden yararlanır.
Kombinasyon tedavisi uygulandıktan sonra hastalar medyan olarak yaklaşık 14 ay yaşadı. Ortalama olarak, hastalık ilerlemesi olmadan yaklaşık 10 ay yaşadılar. Dışkı nakillerinin, tedavisi zor olan bu kanser için çok önemli olan daha sağlıklı bir bağırsak mikrobiyomunu potansiyel olarak restore ederek ilaçların etkinliğini artırdığı görüldü.
MD Anderson Kanser Merkezi’nde gastroenteroloji uzmanı olan Dr. Yinghong “Mimi” Wang, kanser ve tedavilerinin hastaları genellikle enfeksiyonlara ve bazı kemoterapi ve immünoterapi ilaçlarının yaygın bir yan etkisi olan kolit gibi durumlara daha yatkın hale getirdiğini açıklıyor.
Verdiği demeçte, “Kanser hastalarında bağırsak mikrobiyomu, malignite, kanser tedavisi ve antibiyotik maruziyeti gibi çoklu risk faktörleri nedeniyle sıklıkla disbiyoz sergiler. “Sağlıklı donör materyali kullanarak mikrobiyomu doğal olarak değiştiren FMT, immünoterapi kaynaklı kolit için gelecekteki en umut verici tedaviyi temsil ediyor.”
FMT süreci hastanın durumuna göre değişmektedir. Alt gastrointestinal sistem (GI) ile ilgili sorunlar için yöntemler arasında kolonoskopi veya lavman yer alırken, üst GI sistem seçenekleri arasında dondurularak kurutulmuş kapsüller veya beslenme tüpü veya endoskopi yoluyla doğrudan infüzyon yer alıyor. Dr. Wang çoğu hastanın kolonoskopiyi tercih ettiğini belirtiyor.
Dr. Wang, “Verilerimiz FMT’nin hızlı bir başlangıçla güvenli ve etkili bir tedavi olduğunu göstermiştir” dedi. “İshal, kanama, dışkıda mukus veya ağrı gibi kolitle ilişkili olağan semptomlar, fekal transplantasyondan sonraki 4-5 gün içinde tipik olarak düzeliyor veya ortadan kalkıyor.”
Dr. Goodyear, “Bir tedavi olarak fekal transplantasyonun şafağı yeni söküyor” diyor. Devam eden araştırmalar ve artan klinik kanıtlarla birlikte FMT’nin sadece tedavi sonuçlarını iyileştirmek için değil, aynı zamanda kanser hastalarının yaşam kalitesini artırmak için de umut vaat ettiğini söyledi.
Pulse Elektrik Alan Terapisi
Pulse Electric Field (PEF) tedavisi, sağlıklı dokuları korurken hücre zarlarını bozmak için elektrik darbeleri kullanarak kanser hücrelerini hedefler ve yok eder. Bu yöntem ameliyat, kemoterapi ve radyasyon gibi geleneksel tedavilere daha az invaziv ve daha kesin bir alternatif sunuyor.
Dr. Goodyear, “İnsan vücudu savaş alanı ve bağışıklık sistemi de ikincil hasar haline geldi” dedi. “PEF tedavisi, insanı hedef almak yerine tümörü hedef almaya odaklanarak bu paradigmayı değiştiriyor.”
PEF terapisi, elektroporasyon olarak bilinen bir süreç olan iki elektrot arasında kısa, yüksek voltajlı darbeler gönderir. Bu, kanser hücresi membranlarında geçici delikler (gözenekler) oluşturarak terapötik ajanların daha etkili bir şekilde nüfuz etmesini sağlar veya hücrelerin doğrudan ölmesine neden olur.
2023 Scientific Reports çalışması, nano darbeli PEF’in pankreas kanseri hücrelerinde çoklu ilaç direncini azalttığını ve hücreleri kemoterapiye daha duyarlı hale getirdiğini göstermiştir. Tedavi, kanser hücresi kümelerini önemli ölçüde küçülterek tümör büyümesinin azaldığını göstermiştir.
Kaliforniya’daki Williams Kanser Enstitüsü’nde, son gelişmeler arasında daha büyük bir elektrik alan genliği üreten ve kanser hücrelerine daha derinlemesine nüfuz eden nano darbeli PEF yer alıyor. Bu teknik, hücre zarının savunmasını atlayarak iç yapılara zarar verir ve böylece hücre ölümüne yol açar.
Nano darbeli PEF, cerrahi, kemoterapi veya radyasyon için uygun aday olmayan hastalar için tedavi seçenekleri sunmaktadır.” “Bu minimal invaziv tedavi sağlıklı dokuları korur ve iyileşme süresini önemli ölçüde azaltır.”
Kriyoablasyon
Kriyoablasyon, kanserli dokuları yok etmek için aşırı soğuk kullanarak, tümörleri hedef alırken sağlıklı çevre dokuyu koruyan minimal invaziv bir seçenek sunar.
Dr. Goodyear, “Kriyoablasyon, tümörleri ısı veya kimyasallar yerine doğrudan aşırı soğukla hedefleyerek tedavi ortamını değiştiriyor” dedi.
Prosedür, tümöre bir prob yerleştirilmesini ve argon gazı ile hızla soğutulmasını içerir. Kriyoablasyon, hücreler içinde buz kristalleri oluşturarak anında hücre ölümüne yol açar ve ayrıca dondurma işleminin bir parçası olarak apoptoz olarak bilinen programlanmış hücre ölümünü tetikler.
Theranostics’te yayınlanan 2022 tarihli bir çalışma, kriyoablasyonun geleneksel ısı bazlı yöntemlere göre daha hızlı iyileşme süreleri ve daha iyi tümör yanıtı sunduğunu ortaya koymuştur. Doktorlar nanopartiküller kullanarak tümörleri daha hassas bir şekilde hedefleyebilir, bu da tedaviyi daha etkili hale getirir ve yan etkileri azaltır.
Temmuz 2024’te Japon araştırmacılar, IceCure Medical’in ProSense Cryoablation Sistemi ile tedavi edilen meme kanserli kadınların yüzde 99,74’ünde hastalığın geri dönmediğini bildirdi. Japon Meme Kanseri Derneği’nin 32. Yıllık Toplantısı’nda sunulan bulgular, profesör Eisuke Fukuma tarafından yönetilen ve 10 yıl boyunca 389 hastayı kapsayan bir çalışmaya dayanıyordu. Ayrıca, beş yıllık bir takip çalışması, tedavi edilen hastalarda kanserin geri dönmediğini göstermiştir.
Bay Fukuma bir basın açıklamasında “Tümörlerin tedavisindeki büyük etkinliğe ve olumlu kozmetik sonuçlara ek olarak, kriyoablasyonun bağışıklık sistemi üzerinde potansiyel olarak olumlu etkileri olduğuna ve uzun vadeli sonuçları daha da iyileştirdiğine dair kanıtlar var” dedi.
Dr. Goodyear, “Kriyoablasyon sadece kanser hücrelerini öldürmekle kalmıyor, aynı zamanda neoantijenleri serbest bırakarak bağışıklık sistemini de uyarıyor” diyerek bu konuya açıklık getirdi.
Neoantijenler, bir bağışıklık tepkisini tetikleyebilen yeni maddelerdir. Kanser hücreleri kriyoablasyon ve PEF kullanılarak yok edildiğinde, bu yeni antijenleri serbest bırakırlar. Bağışıklık sistemi daha sonra bu antijenleri tanır ve kansere saldırmak için harekete geçer.
Bu tedavi, özellikle ulaşılması zor bölgelerdeki prostat, karaciğer, böbrek, meme ve akciğer kanserleri için özellikle etkilidir. Minimal invaziv doğası, hastalar için daha hızlı iyileşme süreleri anlamına gelir.
İntratümöral İmmünoterapi
İntratümöral immünoterapi, sistemik bir bağışıklık tepkisini tetiklemek için doğrudan tümörleri hedef alır. Annals of Oncology’deki bir makaleye göre, intratümöral immünoterapi, bağışıklık sistemini güçlendirici ajanları doğrudan tümöre enjekte ederek “tümörü kendi aşısı olarak kullanmayı amaçlayan bir terapötik stratejidir”.
İntratümöral immünoterapi genellikle immünoterapi veya kemoterapiyi PEF ve kriyoablasyon gibi tekniklerle birleştirir. Dr. Goodyear’a göre amaç, lokal bağışıklık yanıtını aktive etmek ve kanserle savaşmak için vücudun doğal savunmasını kullanarak bunu tüm vücuda yaymaktır.
Dr. Goodyear, “Vücudun doğasında var olan bağışıklık sistemini, yapmak için yaratıldığı işi yapmak için kullanıyoruz” diye vurguluyor. Radyasyon literatüründe abscopal etki olarak bilinen bu yaklaşımın melanom, baş ve boyun kanseri, meme kanseri, karaciğer kanseri ve prostat kanseri tedavisinde başarılı olduğu kanıtlanmıştır.
SYNC-T, tümörlere saldıran ve bağışıklık sistemini harekete geçiren, kanser hücrelerini yok etmek ve yeni antijenler oluşturmak için kriyoablasyon ile güçlendirilmiş dört tedavinin güçlü bir kombinasyonudur.
Nisan 2024’te Amerikan Kanser Araştırmaları Derneği’nde Dr. Jason Williams, evre IV prostat kanserinde intratümöral SYNC-T için faz I deneme sonuçlarını sundu. Denemede sınırlı seçenekleri olan 13 bakımevi hastası yer aldı ve yüzde 85’i tedaviye yanıt verdi. Beşi tam yanıt verirken altısı kısmi yanıt verdi ve birçoğunun tam yanıta ulaşması bekleniyordu.
Bu terapi, lokal tümör tedavisini SYNC-T’nin bağışıklık sistemini güçlendirerek vücuttaki kanseri tanıması ve onunla savaşması ile birleştirmektedir.
Dr. Goodyear, “Bu, herkese uyan tek tip tedaviden hassas kanser tedavisine devrim niteliğinde bir geçiştir; sadece kansere saldırmayı değil, aynı zamanda vücudunuzun kendi savunmasını savaş için silahlandırmayı vaat eden bir yöntemdir” dedi.
Hedefe Yönelik Ozmotik Litik Tedavi
Hedeflenmiş Ozmotik Litik (TOL) terapi, kanser hücrelerinin içindeki sodyum seviyelerini artırarak hücrelerin parçalanmasına neden olur. Bu yöntem, sağlıklı hücreleri korurken kanser hücrelerini hedef almayı amaçlamaktadır.
Bütünleştirici bir hekim ve İşbirlikçi Tıp Merkezi’nin kurucusu olan Dr. Christine Hauser, TOL’u ayrıntılı olarak tartıştı. Hauser, TOL’un kanser hücrelerindeki belirli sodyum kanallarını açmak için konfluent bir alan ya da bir enerji alanı kullandığını ve bu sayede daha invaziv prosedürlerden ayrıldığını açıkladı. Bu işlemin etkili olabilmesi için önce kalp ilacı Digoxin verilerek sodyum-potasyum pompası kapatılıyor ve hücrelerin sodyumu dışarı atması engelleniyor.
Dr. Hauser ayrıca tüm hücrelerin sodyum kanallarına sahip olmasına rağmen, bazı ilerlemiş kanserlerde bu sayının arttığını açıkladı. TOL kanser hücrelerini daha fazla sodyum emmeye zorlarken, Digoxin normalde sodyumu dışarı atan pompaları bloke eder. Bu sodyum birikimi suyun içeri girmesine ve ozmoz adı verilen bir süreçle patlayana kadar hücrelerin şişmesine neden olur. Bu kanalları hedef alan TOL, teorik olarak sağlıklı hücrelere zarar vermeden kanser hücrelerini yok edebilir.
2021 yılında, ileri derecede skuamöz hücreli serviks karsinomu olan 46 yaşındaki bir kadın, diğer tüm seçenekleri tükettikten sonra TOL ile tedavi edildi. Current Oncology’de yayınlanan bir çalışmaya göre, kadının sadece günler ya da haftalar ömrü kalmıştı.
Hızla ilerleyen kanserine rağmen, tedavi yoğunluğunu azalttı ve muhtemelen tümör ölümüne katkıda bulundu. Yazarlar, “Hasta, tedaviden sonra toplam dokuz hafta, yani beklenenden sekiz haftadan daha uzun bir süre boyunca yaşam kalitesinde iyileşme ile hayatta kaldı” dedi.
Yazarlar, “Bugüne kadar, TOL’un normal dokulara zarar vermeden veya fark edilebilir yan etkiler üretmeden çeşitli ileri karsinom türlerinin boyutunu küçülttüğü ve büyümesini yavaşlattığı ve farelerde ve refakatçi hayvanlarda sağkalımı artırdığı gösterilmiştir” diye yazdı.
TOL tedavisi nispeten yenidir ve tüm kanser türleri için etkili değildir. Hayvan testlerinde umut verici olsa da, henüz Amerika Birleşik Devletleri’nde mevcut değildir. Ancak, TOL’un patentini elinde bulunduran Oleander Medical Technologies, ilk insan denemeleri için onay almak üzere ABD Gıda ve İlaç İdaresi rehberliğinde çalışmaktadır.
Yeniden Tasarlanmış İlaçlar
Yeniden tasarlanmış ilaçlar, kanseri yenilikçi yollarla hedeflemek için eski, patent dışı ilaçları kullanır. Tıpta yeni olmamakla birlikte bu yaklaşım, yeni ilaçlara kıyasla daha düşük geliştirme maliyetleri ve daha kısa onay süreleri nedeniyle onkolojide ilgi görmeye başlamıştır. Bu konsept, 2014 yılında Onkolojide İlaçları Yeniden Tasarlama (ReDO) projesiyle yaygın bir şekilde tanınmıştır.
“Yeniden tasarlanan ilaçlar kanser için bir tedavi ya da geleneksel tedavilerin yerine geçmez. Bunlar, tedavilerin hassas bir şekilde istiflenmesi için değerli yardımcılardır” diye açıklıyor Dr. Goodyear. Bu ilaçlar belirli kanser yollarını etkili bir şekilde hedefleyerek geleneksel tedavilere ek destek sağlayabilir.
Örneğin, Celebrex, ivermektin, düşük doz naltrekson ve Mebendazol gibi ilaçlar artık beyin metastazlı meme kanseri gibi kanserlerin ilerlemesinde rol oynayanlar da dahil olmak üzere kanser hücrelerindeki kritik yolları hedef almak için kullanılıyor.
Aslen Tip 2 diyabet için kullanılan metformin ve ağrı kesici olarak bilinen aspirin, kanser hücresi büyümesini engellemeye ve apoptozu indüklemeye yardımcı olan mekanizmalara sahiptir.
Yeniden tasarlanmış ilaçlar, genleri, proteinleri ve diğer biyolojik faktörleri inceleyen gelişmiş teknikler kullanarak kanser hücrelerini hedefleme konusunda umut vaat etmektedir. Dr. Goodyear, önemli araştırmaların başarılarını desteklediğini söylüyor. Bununla birlikte, etkinliği sağlamak ve “her şeyi duvara fırlatma” yaklaşımının tuzaklarından kaçınmak için kullanımları dikkatle yönetilmelidir.
Sheramy Tsai, BSN, RN, deneyimli bir hemşire
Yorumlar